Ce que nous faisons
Faites équipe avec nous pour maximiser le potentiel de réussite de vos démarches en matière d’essais cliniques!
Nous excellons dans la mise en place d'essais cliniques adaptés aux besoins spécifiques de nos clients pour leurs de dispositifs médicaux, tout en conservant une approche pratique et en mettant l’accent sur la qualité et la conformité. Nous proposons une gamme complète de services, de la conception à la réalisation d'essais cliniques pour les dispositifs médicaux, incluant :
Conception de l’étude clinique

Conception de l’étude clinique
- Élaboration et/ou révision du format et du contenu du protocole d'étude clinique, comprenant des conseils au sujet de la conception de l'étude, des hypothèses et des analyses biostatistiques ;
- Identification des critères d'évaluation clinique pertinents pour la sécurité ou les performances du dispositif; et
- Révision du protocole, du consentement éclairé et de la brochure de l'investigateur pour assurer la conformité aux Bonnes Pratiques Cliniques pour Dispositifs Médicaux selon la norme ISO 14155.
Gestion de projet

Gestion de projet
- Diriger les activités de gestion de projet, assurer la revue et la supervision de l'étude pour les commanditaires pendant l'exécution de toutes les étapes de l'étude ;
- Identifier et sélectionner le(s) prestataire(s) de services cliniques en fonction des besoins en ressources de l'étude (services complets ou personnalisés, fournisseur(s) tiers) ;
- Qualifier le(s) prestataire(s) de services cliniques ; et
- Établir et maintenir le dossier d'essai principal (TMF - Trial Master File)
Soumissions réglementaires et enregistrements

Soumissions réglementaires et enregistrements
- Interactions avec les autorités réglementaires (Organismes Notifiés, Autorités Compétentes Nationales) ;
- Préparation et soumission des demandes pour les Autorisations d'essais cliniques (AEC) auprès de Santé Canada ou des approbations des Dispositifs d'investigation (IDE) auprès de la FDA ;
- Coordination des soumissions initiales et des amendements de protocole auprès des CER (Comités d'Éthique de la Recherche) locaux et/ou centraux ; et
- Enregistrement des études d'investigation dans les registres nationaux (par exemple, clintrials.gov).
Gestion du site et surveillance des études

Gestion du site et surveillance des études
- Identification et/ou sélection du site de l’étude ;
- Formation des équipes du site et de l'étude ;
- Mise en œuvre et rapport de la surveillance de l'étude clinique et ce, à toutes les étapes (initiation, recrutement, clôture) ; et
- Soutien lors des inspections des autorités règlementaires.
Audit et qualification des fournisseurs

Audit et qualification des fournisseurs
- Audit du site d'étude clinique ;
- Audit des procédures cliniques ;
- Identification et qualification des fournisseurs de services (laboratoires, logistique, transport, etc.) ; et
- Audit des fournisseurs de services.
Rapport relatif à la sécurité

Rapport relatif à la sécurité
- Élaborer et examiner le plan de notification de sécurité de l'étude et les formulaires pour garantir la conformité aux réglementations applicables en matière de notification des incidents pour les dispositifs médicaux ;
- Soutenir les commanditaires dans la réception, l'examen et le traitement des informations relatives aux incidents pour garantir des notifications obligatoires en temps opportun, le cas échéant ; et
- Soumettre les rapports d'événements indésirables graves (SAE) et/ou les rapports d'événements indésirables associés à un dispositif (ADE) de manière accélérée et conformément aux exigences des autorités réglementaires.
Laboratoire d’analyse d’images (Corelab)
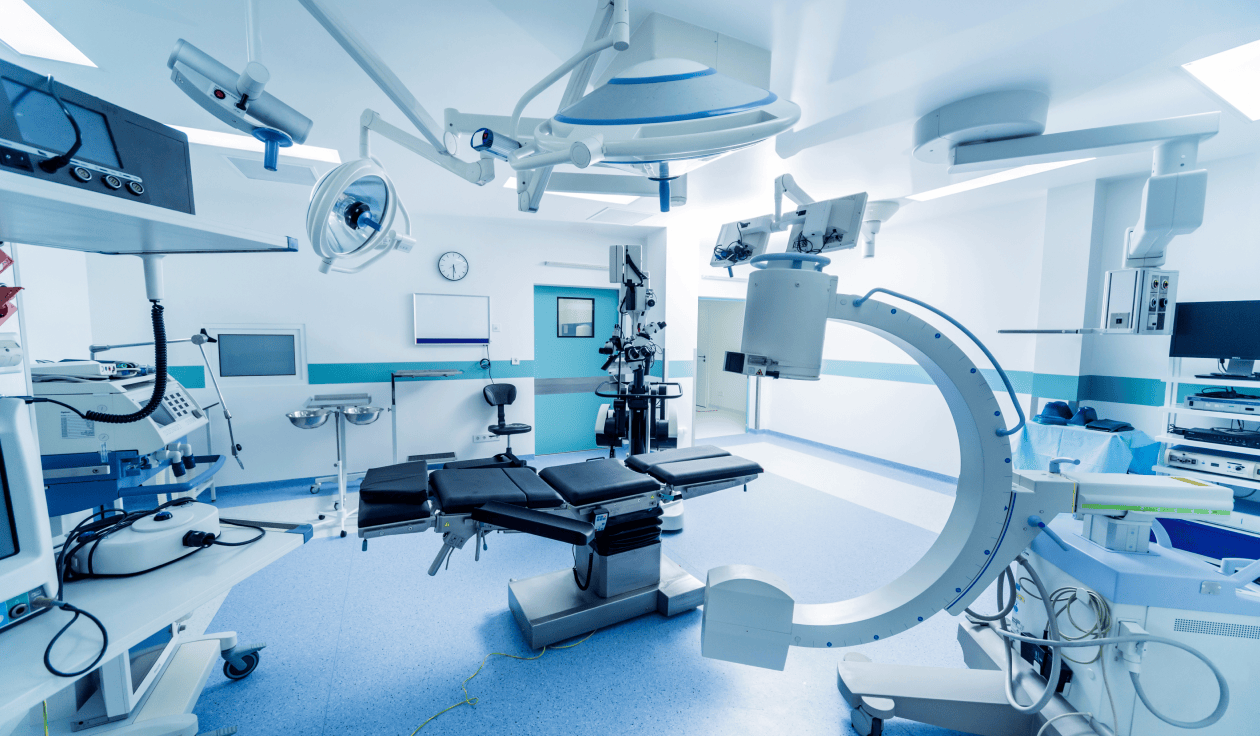
Laboratoire d’analyse d’images (Corelab)
Nous offrons un éventail complet de services de laboratoire pour l’analyse d’images avec des solutions d'imagerie adaptées aux besoins spécifiques de nos clients.
Grâce à notre partenariat avec Beam Radiology, nous fournissons une suite complète de services d'imagerie médicale avec interprétation rapide, en utilisant des instruments et des technologies de pointe, pour améliorer et accélérer le développement de dispositifs médicaux ; le tout parfaitement intégré au flux de travail de l’essai clinique.
Qualité

Qualité
Aide à la rédaction, à l’exécution et à maintenir la qualité
La qualité du travail est directement liée à la conformité réglementaire. En partenariat avec LOK North America, nous nous engageons à fournir un travail de la plus haute qualité. En tirant parti du système de gestion de la qualité de LOK North America entièrement certifié selon les normes et les exigences de MDSAP ISO 13485, nous supervisons attentivement chaque projet. Cela inspire un niveau accru de confiance dans notre capacité à respecter et à maintenir de manière constante les exigences réglementaires, garantissant ainsi l'achèvement en temps voulu et l'allocation efficace des ressources.
Conformité réglementaire
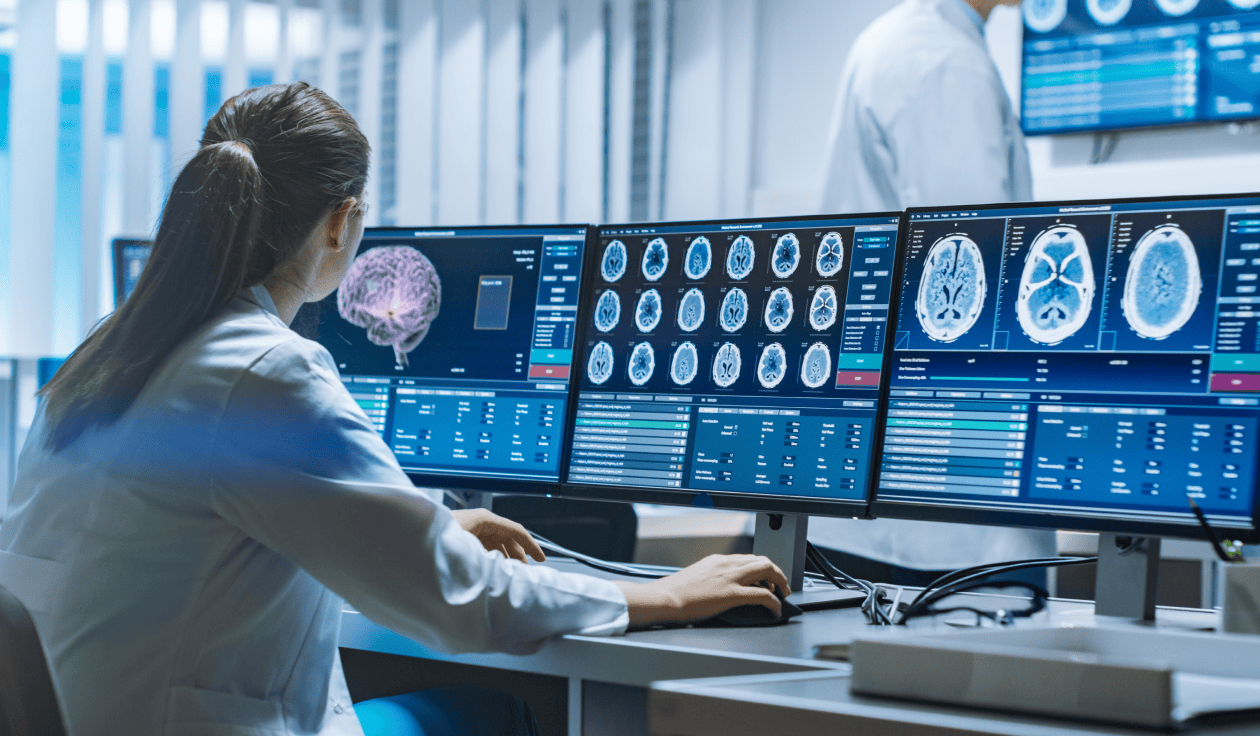
Conformité réglementaire
Optimisez votre stratégie de recherche clinique
Grâce à notre partenariat avec LOK North America, nous proposons une vaste gamme de services-conseils sur les instruments médicaux et de solutions réglementaires afin d’aider nos clients à s’y retrouver dans le cadre réglementaire pertinent et à se conformer aux exigences de la Loi sur les aliments et drogues et du Règlement sur les instruments médicaux.
Nous nous engageons à fournir un soutien à nos clients et à offrir une expertise inégalée afin d’élaborer une stratégie réglementaire adaptée pour leurs dispositifs médicaux.
Ce que nous accomplissons le mieux
Une approche globale soutenue par des services spécialisés afin d’encadrer les exigences uniques et complexes tout au long du cycle de vie, et ce, pour chaque catégorie de dispositif médical.
Nous offrons à nos clients l'avantage d'une vaste expérience collective lors de la formulation et de la mise en œuvre des stratégies réglementaires et des conceptions d'études. Nos spécialités thérapeutiques incluent :
- Chirurgie générale et plastique
- Dispositifs pour la colonne vertébrale
- Santé numérique et imagerie
- Cardiologie
- Dispositifs de diagnostic in vitro
- Soins des plaies et dermatologie
- Dispositifs dentaires
En réalisant des synergies, l’alliance stratégique entre Beam Radiology, LOK North America et ViaClinica offre une solution complète pour les start-ups, les entreprises de taille moyenne et les multinationales. Grâce à notre approche, vous aurez un accès complet à toute l’information nécessaire, éliminant ainsi le besoin de coordonner et gérer plusieurs consultants.


À propos de nous
Un guichet unique pour les essais cliniques
ViaClinica est une organisation de recherche contractuelle (ORC) offrant des services complets dédiés à la réalisation et à la gestion d'essais cliniques au nom de commanditaires dans le domaine des dispositifs médicaux. Le siège social de ViaClinica est situé à Calgary, au Canada, avec un bureau satellite dans la région du Grand Montréal, au cœur de l'environnement des sciences de la vie.
ViaClinica travaille en collaboration avec des partenaires pour promouvoir la recherche clinique de haute qualité et selon les meilleurs pratiques de l’industrie. Avec la forte conviction que l'ensemble est plus grand que la somme de ses parties, l'expertise combinée de nos professionnels chevronnés, forme un savoir collectif essentiel à la création de valeur, qui vous aide à planifier et à exécuter chaque étape des essais cliniques de vos dispositifs au Canada ou ailleurs. Notre équipe possède d’excellents antécédents éprouvés en matière d’essais monocentriques, premiers essais chez l'humain, de faisabilité, multicentriques, pilotes, pivots et post-commercialisation, qui garantissent la protection des patients et la conformité réglementaire par le biais de la surveillance clinique, de l'audit, de la formation, de la gestion de projet et de la materiovigilance.
Contactez-nousContactez-nous
Surmonter les défis considérables que représente la réalisation des essais cliniques
Avez-vous des questions, des suggestions ou avez-vous besoin de plus d'informations ?
587-885-2988